Вопрос № 1 Строение атома
по количеству дуг можно определить номер периода элемента ( в данном случае второй период)
по количеству электронов на последнем уровне (последней дуге) определяем номер группы, в которой находится элемент (в данном случае пятая группа)
по сумме электронов на всех уровнях определяем порядковый номер элемента ( в данном случае седьмой номер)
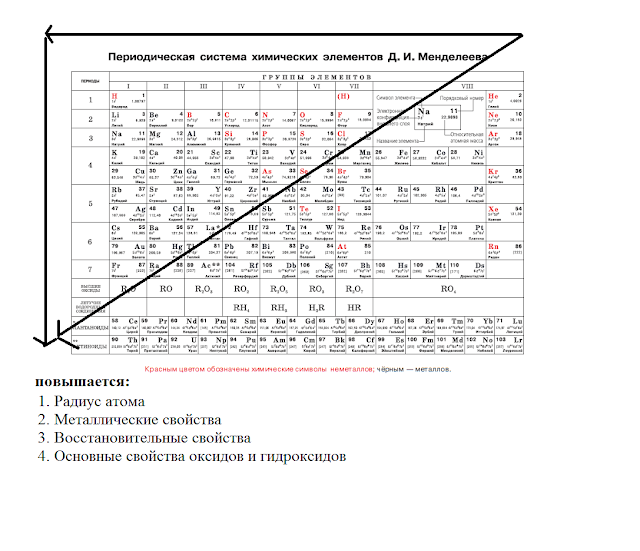
Вопрос № 2 Периодическая система химических элементов
Вопрос № 4 Степень окисления
Номер периода показывает количество энергетических уровней в атоме.
Номер группы показывает количество электронов на внешнем уровне у элементов главных подгрупп, а также максимальную степень окисления данного элемента (исключение фтор и кислород).
Порядковый номер элемента показывает: 1) заряд ядра атома; 2) количество протонов; 3) количество электронов.
Количество нейтронов находят по разности относительной атомной массы и заряда ядра атома (порядкового номера).
Пример:
по количеству дуг можно определить номер периода элемента ( в данном случае второй период)
по количеству электронов на последнем уровне (последней дуге) определяем номер группы, в которой находится элемент (в данном случае пятая группа)
по сумме электронов на всех уровнях определяем порядковый номер элемента ( в данном случае седьмой номер)
Вопрос № 2 Периодическая система химических элементов
Вопрос № 3 Виды химической связи
Вопрос № 4 Степень окисления
Правила определения степени окисления
1.Степень окисления в простом
веществе равна нулю.
2.Постоянная степень окисления:
а) 1 группа +1 (искл. Н с металлами -1, с неметаллами +1;
Cu +1, +2)
б) 2 группа +2
в) 3 группа +3
г) F -1
д) О -2, но может быть -1, +2,
-1/2
3.Максимальная положительная
степень окисления элементов главных подгрупп равна номеру группы.
4. Максимальная отрицательная
степень окисления элементов главных подгрупп равна номеру группы-8.
5.Сумма степеней окисления в
молекуле равна нулю, а в ионе – заряду этого иона.
В
Вопрос № 5 Классификация неорганических веществ
Оксиды
Оксиды - это сложные вещества, состоящие из двух элементов, один из которых кислород в степени окисления -2
Если к формуле оксида присоединить молекулу воды, то мы получим гидроксид (основание, амфотерный гироксид или кислоту)
Основному оксиду будет соответствовать основание, амфотерному оксиду -амфотерный гидроксид, кислотному оксиду- кислота.Для того, чтобы понять какому оксиду какой гидроксид соответствует нужно расставит степени окисления в оксиде и гидроксиде. В соответствующих друг другу оксиде и гидроксиде они должны совпадать.
Например:
Даны оксиды
CrО3, Cr2О3,CrО
и гидроксиды
Н2Cr2О7,Cr(ОН)2,Cr(ОН)3
Необходимо определить какой гидроксид какому оксиду соответствует. Для этого находим степени окисления хрома во всех соединениях
Cr +6О3, Cr2+3О3, Cr+2О
Н2Cr2+6О7,Cr+2(ОН)2,Cr+3(ОН)3
получаем:
Н2Cr2+6О7 соответствует Cr +6О3
Н2Cr2+6О7 соответствует Cr +6О3
Cr+2(ОН)2 соответствует Cr+2О
Вопрос № 6 Вычисление массовой доли элемента в молекуле









Комментариев нет:
Отправить комментарий